suscripción
suscripción
Cierta Ciencia
En Cierta Ciencia, de la mano de la genetista Josefina Cano nos acercamos, cada quince días, al trabajo de muchos investigadores que están poniendo todo su empeño en desenredar la madeja de esa complejidad que nos ha convertido en los únicos animales que pueden y deben manejar a la naturaleza para beneficio mutuo. Hablamos de historias de la biología.
Sí a la edición genética, no a las fantasías.
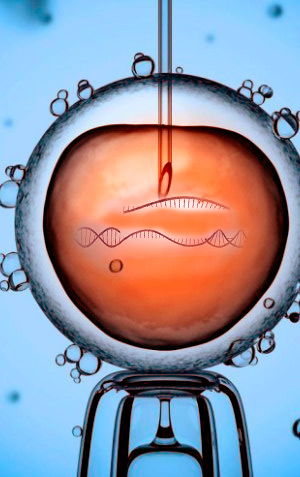
La noticia científica más notable de la primera semana de agosto del pasado 2017, al menos porque ha levantado una polvareda por sus implicaciones éticas, ha sido la de la utilización de la nueva técnica de edición de genes, CRISPR (1) en embriones humanos. El objetivo del estudio fue modificar un gen patógeno, gen que en la vida adulta ocasiona una cardiomiopatía.
Los investigadores, de la Universidad de Oregon, liderados por Shoukhrat Mitalipov, utilizaron espermatozoides de un hombre con la cardiomiopatía para fertilizar los óvulos de 12 mujeres saludables, adicionando luego CRISPR, las tijeras genéticas que cortaron la secuencia mutada del hombre, en un único gen que causa la enfermedad (2).
Inyectaron también una secuencia de ADN sintético sano, esperando que el genoma del hombre, con el hueco dejado por el corte, lo rellenaría con ese ADN sano tomándolo como molde. Así es como este proceso de edición genética (corta y pega) trabaja en otras células del cuerpo y en embriones de ratón.
Sin embargo, el gen copiado fue el del óvulo, dejando a los científicos sin explicación, aunque lo más probable es que las células sexuales o gametos hayan evolucionado para auto repararse porque son las únicas células que transmiten los genes a sus descendientes y necesitan y poseen una protección especial.
Después de varios ensayos con resultados ambiguos, los investigadores descubrieron que lo mejor era adicionar el CRISPR al momento de la fertilización. Así obtuvieron 42 de 58 embriones, 72% con dos copias libres de la mutación en cada célula del embrión. Los embriones fueron destruidos tres días después. El método no fue perfecto pues los otros 16 embriones tuvieron alteraciones en su ADN, aunque uno de los miembros del equipo señala que con más tiempo y trabajo se podría llegar a un 90% de embriones sin la mutación.
Cuando la enfermedad está causada por genes defectuosos en el genoma materno, puede ocurrir el mismo proceso, con la secuencia genética sana del hombre sirviendo como molde. ¿Pero y qué si ambos padres tienen la mutación? Ahí se tendría que forzar a la utilización de un ADN sintético sano. Un problema complicado por lo que se anotaba antes.
La euforia provocada por este estudio, apenas en pañales, ha llevado a titulares tan sensacionalistas y fantasiosos como el señalar que 10.000 enfermedades causadas por un único gen, con una frecuencia muy baja en la población al punto de llamarlas raras, se vayan a eliminar con esta técnica, no deja de sembrar dudas.
Pero que es importante y mucho, lo es. Podría ser de muchísima utilidad para iluminar ese campo tan oscuro hasta ahora, (el 50% de los embriones se elimina de forma natural) de los problemas de infertilidad y de las pérdidas continuas en mujeres sanas. Y cuando en una familia circulan genes que ocasionan sufrimientos enormes, el poder editarlos sería un gran alivio.
Quienes se sometan a este tratamiento razones de peso tendrán, no lo harán por motivos triviales. El sexo es gratis y más divertido que someterse a los dolores de la Fertilización in Vitro, proceso obligado para la edición genética, por lo que solo los necesitados de verdad querrán a sus bebés “editados”.
Ahora bien. La posibilidad de utilizar la técnica para otros fines diferentes al de remediar enfermedades inhabilitantes y dolorosas, todas ellas ocasionadas por la alteración de un gen único, corre más bien por cuenta de la ciencia ficción.
La altura de las personas es una característica gobernada por muchos genes. Un estudio reciente (3) informa que existen hasta 700 variantes genéticas de las cuales 683 ya han sido identificadas. Pretender fabricar bebés editados para que sean atletas de élite, ¡hay que ver! Las personas que se ganan todas esas medallas de oro con seguridad tienen una colección de variantes genéticas propicias para tal propósito. Selección y adaptación.
Y lo mismo ocurre con la inmensa mayoría de las características buenas o malas de las personas. Los talentos y las dolencias del cerebro son de una complejidad enorme, donde los genes actores siguen un guión que no es un mensaje (tan de moda ahora) de 140 caracteres, sino que se guían por todo un escrito robusto, con notas y recomendaciones y que además se verá modificado, embellecido o arruinado por la interacción con los otros actores en un escenario, para nuestro caso el micro ambiente celular.
Así, la edición de embriones humanos tiene una probabilidad de éxito muy baja para prevenir la mayoría de los problemas médicos.
Y aquí, cada vez que lo necesitamos aparece Siddhartha Mukherjee.
“En las primeras décadas del siglo XXI estamos aprendiendo a hablar un nuevo lenguaje de causa y efecto y estamos construyendo una nueva epidemiología de nosotros mismos: estamos empezando a describir enfermedad, identidad, afinidad, temperamento, aficiones –y al final, destino y azar– en términos de genes y genomas. Esto no es hacer el absurdo reclamo de que los genes son los únicos lentes a través de los que los aspectos fundamentales de la naturaleza y el destino se pueden mirar. Pero es proponer y considerar en serio una de las más provocativas ideas sobre nuestra historia y futuro: la influencia de los genes en nuestras vidas es más rica, más profunda y más enervante de lo que habíamos pensado. Esta idea se vuelve aún más provocativa y desestabilizadora a medida que aprendemos a entender, alterar y manipular el genoma de manera intencional, adquiriendo la habilidad de cambiar hechos futuros y escogencias”.
¿Será que esos nuevos conocimientos llevarán a otras formas de empatía y entendimiento? O se convertirán en nuevas formas de discriminación. Eso solo se sabrá siguiendo de cerca el desarrollo de los estudios que ya han echado a andar y que no se van a detener, por fortuna, y estableciendo marcos de regulación sensatos y basados siempre, siempre, en la ciencia, que no en presiones externas o en las opiniones de los miles de comités de ética, que, cómo no, ya proliferan para el caso y que casi siempre caen en el precipicio de la burocracia.
Referencias.
(1) http://ciertaciencia.blogspot.com.co/2015/11/crispr-editando-nuestros-genes.html
(2) Correction of a pathogenic gene mutation in human embryos.
Ma H., et al. Nature 2017.
(3) Rare and low-frequency coding variants alter human adult height.
Marouli E., et al. Nature, 2017.
Más información en el Blog de Josefina Cano: Cierta Ciencia
Nuestros programas
- Hablando con Científicos
- Vanguardia de la Ciencia
- Ulises y la Ciencia
- Ciencia y genios
- Ciencia Nuestra de cada Día
- Zoo de fósiles
- Seis patas tiene la vida
- Océanos de Ciencia
- Quilo de Ciencia
- Ciencia EXtrema
- El Neutrino
- Cierta Ciencia
- Ciencia Fresca
Podcasts
Ciencia con Humor
Recomendamos
- El Neutrino
- Blog de divulgación científica de Jorge Laborda
- Cierta Ciencia
- La Aldea Irreductible
- La Buhardilla 2.0
- Aragosaurus
- El podcast del microbio
- Hablando de Ciencia
- Glosopetrae
- Podcast Coffee Break
- Twinkl Blog educativo en español
- El Pintor de las Sombras
- AstroAfición
- Blog de Laboratorio
- Locuciencia
- Noticias de la Ciencia y la Tecnología
![]()
Apoya a CienciaEs haciéndote MECENAS con una donación periódica o puntual.

40,8 millones de audios servidos desde 2009
Agradecemos la donación de:
Maria Tuixen Benet
“Nos encanta Hablando con Científicos y el Zoo de Fósiles. Gracias.”
Daniel Dominguez Morales
“Muchas gracias por su dedicación.”
Anónimo
Jorge Andres-Martin
Daniel Cesar Roman
“Mecenas”
José Manuel Illescas Villa
“Gracias por vuestra gran labor”
Ulrich Menzefrike
“Donación porque me gustan sus podcasts”
Francisco Ramos
Emilio Rubio Rigo
Vicente Manuel CerezaClemente
“Linfocito Tcd8”
Enrique González González
“Gracias por vuestro trabajo.”
Andreu Salva Pages
Emilio Pérez Mayuet
“Muchas gracias por vuestro trabajo”
Daniel Navarro Pons
“Por estos programas tan intersantes”
Luis Sánchez Marín
Jesús Royo Arpón
“Soy de letras, sigo reciclándome”
Fernando Alejandro Medina Vivanco
“Ayuda”
Anónimo
Fernando Vidal
José V González F
“A nombre de mi hijo León Emiliano hacemos esta pequeña aportación. Escuchar ciencia juntos nos hace muy felices. Gracias.”
Javier Galán Cantero
“Por los grandes programas, gracias”