suscripción
suscripción
Hablando con Científicos
El conocimiento científico crece gracias a la labor de miles de personas que se esfuerzan, hasta el agotamiento, por encontrar respuestas a los enigmas que plantea la Naturaleza. En cada programa un científico conversa con Ángel Rodríguez Lozano y abre para nosotros las puertas de un campo del conocimiento.
Átomo a la vista. Hablamos con Rubén Pérez.
Todo lo que nos rodea, incluidos nosotros mismos, está formado por átomos. Cualquier criatura, por muy pequeña que ésta sea, contiene una cantidad inmensa de esas diminutas unidades básicas. Y la palabra “inmensa” expresa pobremente la realidad porque esconde cifras que contienen muchos ceros, por ejemplo, el número de átomos que se agrupan para dar cuerpo a una persona de unos 60 kilogramos, tiene que ser escrita con un dígito ¡seguido de 27 ceros!. Por mucho que intentemos leer una cifra así, jamás lograremos hacernos una idea de lo “inmensa” que es en realidad.
Tamaño de los átomos.
Si esa cantidad tan impresionante de ceros sirve para hacemos una idea de los átomos que forman nuestro cuerpo, lo cierto es que poco nos dice del tamaño de cada uno de ellos, sólo podemos deducir que son muy pequeños. Los científicos han calculado el tamaño de un átomo de varias maneras y han llegado a la conclusión de que su diámetro (considerado como una esfera) varía entre 0,1 y 0,5 nanómetros. Tampoco esto aclara mucho las cosas porque es muy difícil hacerse una idea de la dimensión real de un nanómetro. Intentémoslo con unos ejemplos.
En el programa de hoy les proponemos un experimento casero: Si tiene a mano un bolígrafo de punta fina, ponga la punta suavemente en contacto con un papel de forma que deje sobre él un punto lo más pequeño posible. Ese punto apenas tendrá una décima de milímetro de diámetro. Pues bien, para cubrir ese diámetro con átomos colocados en fila india necesitaríamos nada menos que alrededor de un millón de ellos. Otro ejemplo, si no tienen a mano un bolígrafo, quítense un cabello, córtenlo con una cuchilla, la sección de ese pelo será un círculo pequeñísimo cuyo diámetro también se puede cubrir con un número de átomos que ronda el millón.
No se pueden dar medidas exactas de las dimensiones de un átomo. Aunque nos lo imaginemos como bolitas compactas con una superficie definida – así lo representan muchos libros de texto -, la realidad es que se pueden describir como un espacio práticamente vacío limitado por una neblinosa y extremadamente tenue nube formada por electrones en movimiento. La mayor parte de la masa de un átomo está en el núcleo y éste es tan pequeño respecto al tamaño del átomo que , como un profesor mío decía, apenas ocupa en su interior lo que una mosca dentro de una catedral. Alrededor se sitúan los electrones, más pequeños todavía, formando con su movimiento una nube borrosa sin límites definidos.
¿Cómo se midió el tamaño de un átomo?
Los científicos han medido el tamaño de los átomos de varias formas. Si el átomo es metálico, dado que en los metales, en estado sólido, estos se apilan muy juntos, se midió la distancia entre dos núcleos y así se calculó el radio de cada átomo. En los no metales, se hizo lo mismo pero escogiendo la distancia entre los núcleos de dos átomos unidos formando una molécula covalente.
Hay diferencias de tamaño entre unos átomos y otros. Un átomo de hidrógeno, el más elemental de todos, sólo tiene un protón en el núcleo y un electrón moviéndose alrededor, en cambio, uno de plutonio (el más estable) tiene un núcleo 244 veces más masivo que el hidrógeno y 94 electrones moviéndose alrededor. Sin embargo, dado que cuanto mayor es el núcleo con más fuerza atrae a los electrones, la nube que éstos forman es más compacta y el radio de un átomo de plutonio es tan sólo 6 veces mayor que el del hidrógeno.
Una vez que ha quedado claro lo pequeñísimo que es un átomo, se pueden imaginar lo extremadamente difícil que es “ver” uno de ellos. Una lupa nos permite aumentar el tamaño de las cosas gracias que sus átomos están exquisitamente situados de manera que curvan los rayos de luz y nos permiten ver las cosas más grandes. Sin embargo, una lupa está hecha de átomos y cuando se pretende ver un átomo individual no sirve para nada.
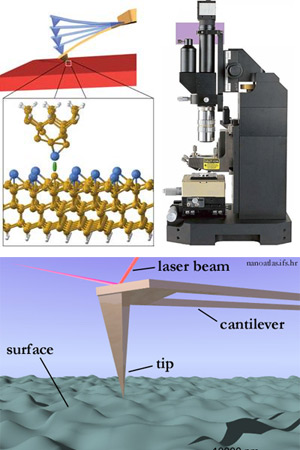
A pesar de la dificultad, los científicos lo han conseguido utilizando el “Microscopio de fuerzas atómicas” un aparato cuyo funcionamiento nos explica nuestro invitado de hoy, D. Rubén Pérez, profesor en el Departamento de Física Teórica de la Materia condensada de la Universidad Autónoma de Madrid. D. Rubén Pérez y su grupo de investigación han conseguido, junto a un equipo multinacional y multidisciplinar de investigadores, verdaderas proezas en este campo durante los últimos años, entre ellas, la identificación de átomos individuales en una superficie y la manipulación de estos átomos hasta el punto de poder cambiarlos de posición y ordenarlos a voluntad. Pero lo más impresionante de estas técnicas está por venir. Escuchen a D. Rubén Pérez.REFERENCIAS
Scanning Probe Microscopy Theory & Nanomechanics Group Forces and Transport in Nanostructures
Y. Sugimoto, P. Jelinek, P.Pou, M. Abe, R. Pérez, S. Morita and O. Custance
Chemical identification of individual surface atoms by atomic force microscopy Nature 446 , 64-67 (2007).
It is possible to write with atoms using an Atomic Force Microscope
Nuestros programas
- Hablando con Científicos
- Vanguardia de la Ciencia
- Ulises y la Ciencia
- Ciencia y genios
- Ciencia Nuestra de cada Día
- Zoo de fósiles
- Seis patas tiene la vida
- Océanos de Ciencia
- Quilo de Ciencia
- Ciencia EXtrema
- El Neutrino
- Cierta Ciencia
- Ciencia Fresca
Podcasts
Ciencia con Humor
Recomendamos
- El Neutrino
- Blog de divulgación científica de Jorge Laborda
- Cierta Ciencia
- La Aldea Irreductible
- La Buhardilla 2.0
- Aragosaurus
- El podcast del microbio
- Hablando de Ciencia
- Glosopetrae
- Podcast Coffee Break
- Twinkl Blog educativo en español
- El Pintor de las Sombras
- AstroAfición
- Blog de Laboratorio
- Locuciencia
- Noticias de la Ciencia y la Tecnología
![]()
Apoya a CienciaEs haciéndote MECENAS con una donación periódica o puntual.

40,8 millones de audios servidos desde 2009
Agradecemos la donación de:
Maria Tuixen Benet
“Nos encanta Hablando con Científicos y el Zoo de Fósiles. Gracias.”
Daniel Dominguez Morales
“Muchas gracias por su dedicación.”
Anónimo
Jorge Andres-Martin
Daniel Cesar Roman
“Mecenas”
José Manuel Illescas Villa
“Gracias por vuestra gran labor”
Ulrich Menzefrike
“Donación porque me gustan sus podcasts”
Francisco Ramos
Emilio Rubio Rigo
Vicente Manuel CerezaClemente
“Linfocito Tcd8”
Enrique González González
“Gracias por vuestro trabajo.”
Andreu Salva Pages
Emilio Pérez Mayuet
“Muchas gracias por vuestro trabajo”
Daniel Navarro Pons
“Por estos programas tan intersantes”
Luis Sánchez Marín
Jesús Royo Arpón
“Soy de letras, sigo reciclándome”
Fernando Alejandro Medina Vivanco
“Ayuda”
Anónimo
Fernando Vidal
José V González F
“A nombre de mi hijo León Emiliano hacemos esta pequeña aportación. Escuchar ciencia juntos nos hace muy felices. Gracias.”
Javier Galán Cantero
“Por los grandes programas, gracias”