suscripción
suscripción
Quilo de Ciencia
El quilo, con “q” es el líquido formado en el duodeno (intestino delgado) por bilis, jugo pancreático y lípidos emulsionados resultado de la digestión de los alimentos ingeridos. En el podcast Quilo de Ciencia, realizado por el profesor Jorge Laborda, intentamos “digerir” para el oyente los kilos de ciencia que se generan cada semana y que se publican en las revistas especializadas de mayor impacto científico. Los temas son, por consiguiente variados, pero esperamos que siempre resulten interesantes, amenos, y, en todo caso, nunca indigestos.
¿Por qué veinte?
Como ya deben saber los oyentes habituales de Quilo de Ciencia, que me consta que alguno hay, normalmente me ocupo aquí de explicar uno de los últimos avances de la ciencia que me ha parecido más importante, más curioso, o simplemente más fácil de explicar.
Sin embargo, de vez en cuando me gusta pararme y reflexionar sobre lo que se conoce, e intentar desvelar las razones de por qué las cosas son así, y no de otro modo. Encontrar una razón, si es posible bien documentada, para las cosas me produce un placer intelectual que considero sólo podemos experimentar nosotros, los humanos. Es éste el placer que deseo compartir contigo, amable oyente. De hecho, también pretendo compartirlo con quienes no tienen más remedio que escucharme, y por ello, una de las primeras lecciones que doy a mis alumnos de Bioquímica de los estudios de Medicina para introducirles por el fascinante camino de la ciencia es incitarles a formular y procurar responder preguntas sobre el mundo que les rodea. La ciencia nunca hubiera surgido si alguien, alguna vez, no se hubiera formulado preguntas como: ¿por qué el cielo es azul?, ¿Por qué el arco iris es un arco, y no un cuadrado? Nada más caen en mis garras (intelectuales), intento que los futuros médicos no crean que las cosas son porque sí, como una vez me respondió una alumna, o porque así las dice el libro o el profesor de turno, sino que piensen que posiblemente tienen una razón de ser que es posible y debemos descubrir.
Con esta intención es con la que les formulo preguntas como ¿por qué las proteínas están formadas por veinte aminoácidos, en lugar de serlo por cuarenta o por sólo diez? De este interesante tema me gustaría hablar hoy. Un tema de ciencia básica, pero que nos puede enseñar muchas cosas sobre el mundo y sobre la vida.
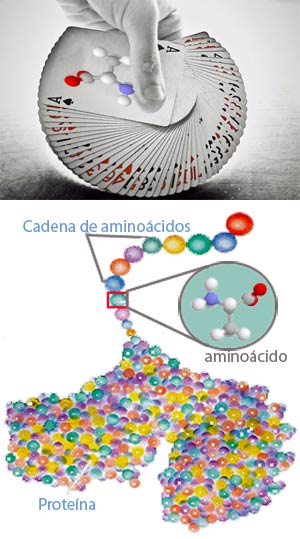
Probablemente sabes ya que las proteínas son las moléculas encargadas del funcionamiento de los procesos vitales. Ellas son las que confieren la estructura a nuestros cuerpos y células y las que participan como herramientas en el control y regulación de todas las reacciones químicas de la base de la vida. Estas interesantísimas moléculas son polímeros, es decir, se forman por la unión de muchas moléculas pequeñas que se unen como si se tratara de los eslabones de una cadena. Las moléculas pequeñas que forman la cadena son los aminoácidos. Así pues, los aminoácidos se unen unos con otros y forman las cadenas moleculares que son las proteínas. Estas cadenas pueden tener un número muy variable de eslabones, y hay proteínas formadas por menos de cien, o proteínas formadas por miles de aminoácidos unidos entre sí.
Los aminoácidos son moléculas de la misma familia. Están formados por la unión de tres grupos químicos, un grupo amino (NH2), un grupo ácido (COOH), de los que reciben su nombre, separados por un grupo químico en el medio. Estos grupos químicos, formados por la unión de diversos átomos de carbono, hidrógeno, oxígeno, nitrógeno o azufre, son los que confieren las propiedades particulares a cada aminoácido. Existen veinte diferentes grupos químicos en los aminoácidos que forman las proteínas y por eso se dice que existen veinte aminoácidos diferentes.
Los grupos químicos proporcionan distintas propiedades a cada aminoácido. Así, los hay que tienen carga eléctrica positiva, y los hay con carga eléctrica negativa; los hay con aversión al agua (hidrófobos) y los hay con afinidad por el agua (hidrófilos); los hay grandes, y los hay pequeños.
Al unirse entre sí para formar las cadenas de proteínas, las propiedades químicas de cada aminoácido que se une a la cadena van a participar en cómo esa cadena molecular, una vez acabada, se retuerce, se pliega en el medio acuoso celular. Y es que la cadena de aminoácidos no se queda estirada, como si se tratara de una cadena de la medalla colgada al cuello, sino que se pliega y adopta diversas formas, como las puede adoptar una cadena depositada sobre la palma de nuestra mano. El plegamiento de esta cadena de aminoácidos es muy importante, porque va a determinar la forma, la estructura de la proteína y este plegamiento depende de las propiedades químicas de los aminoácidos. Así un aminoácido hidrófilo tendrá tendencia a estar cerca del agua, esto es, en la superficie de la estructura plegada, mientras que un aminoácido hidrófobo tenderá a esconderse del agua situándose en el interior de la cadena plegada.
Al plegarse según las propiedades de cada aminoácido, las proteínas adquieren diversas formas que tienen que ver con cómo van a funcionar estas moléculas dentro de la célula. Así, por hacer una analogía fácil, al plegarse, algunas proteínas van a adquirir la forma de una tuerca, otras las de llave inglesa, otras las de clavos y otras las de martillos. Es decir, las proteínas van a convertirse en las diversas herramientas y partes que hacen funcionar a la célula.
Es evidente que si contáramos con sólo un aminoácido, las proteínas no podrían adquirir la diversidad de formas necesaria para convertirse en distintas herramientas y partes. Sólo con una tuerca no podemos construir un motor. De la misma manera con sólo un aminoácido, la cadena tendría un número muy limitado de maneras de plegarse, que dependerían exclusivamente del número de ese único aminoácido que se unieran entre sí. Es decir, con uno, o con muy pocos aminoácidos, las proteínas no podrían producir las diversas piezas necesarias para que el motor celular funcione. Esto sólo es posible si existe suficiente diversidad química en los aminoácidos. Por eso existen unos cuantos diferentes.
Lo anterior explica por qué deben existir más de uno o dos aminoácidos diferentes, pero; ¿por qué veinte y no cuarenta, o sesenta?. Es posible que con mayor número de aminoácidos la diversidad de las proteínas pudiera aumentar. Sin embargo, cada molécula que nuestras células deben manejar cuesta energía para producirla, o conseguirla mediante la dieta. A lo largo de la evolución, los organismos han sufrido pues dos presiones contrapuestas. Por un lado aquellos que fueran capaces de manejar mayor número de aminoácidos tendrían la ventaja de producir proteínas más variadas con funciones más diversas, lo que les permitiría sobrevivir mejor. Por otro, la cantidad de energía necesaria para gestionar la variedad de aminoácidos iría en aumento a medida que éstos también aumentaran en número.
Por consiguiente, al final de millones de años de evolución se llega a un equilibrio. Los organismos disponen del número de aminoácidos diferentes y con la variedad química suficiente para producir una gran diversidad de proteínas, y esto al menor coste energético y de recursos. Un análisis de las estructuras de los aminoácidos nos indica que, en efecto, con veinte diferentes se consigue un abanico bastante completo de posibilidades químicas, muy probablemente el mínimo necesario para producir el máximo de diversidad proteica, es decir, de diversidad de estructuras funcionales posibles.
Por tanto, un análisis científico de la realidad molecular de la vida nos indica que posiblemente las cosas no hubieran podido ser de otra manera. Y hay una buena razón para que así sea. Esta conclusión es intelectualmente mucho más satisfactoria que la de creer o aceptar que las cosas son porque son, conclusión que es válida para aspectos moleculares de la vida y también para cualquier aspecto de la vida cotidiana.
Nuestros programas
- Hablando con Científicos
- Vanguardia de la Ciencia
- Ulises y la Ciencia
- Ciencia y genios
- Ciencia Nuestra de cada Día
- Zoo de fósiles
- Seis patas tiene la vida
- Océanos de Ciencia
- Quilo de Ciencia
- Ciencia EXtrema
- El Neutrino
- Cierta Ciencia
- Ciencia Fresca
Podcasts
Ciencia con Humor
Recomendamos
- El Neutrino
- Blog de divulgación científica de Jorge Laborda
- Cierta Ciencia
- La Aldea Irreductible
- La Buhardilla 2.0
- Aragosaurus
- El podcast del microbio
- Hablando de Ciencia
- Glosopetrae
- Podcast Coffee Break
- Twinkl Blog educativo en español
- El Pintor de las Sombras
- AstroAfición
- Blog de Laboratorio
- Locuciencia
- Noticias de la Ciencia y la Tecnología
![]()
Apoya a CienciaEs haciéndote MECENAS con una donación periódica o puntual.

40,8 millones de audios servidos desde 2009
Agradecemos la donación de:
Maria Tuixen Benet
“Nos encanta Hablando con Científicos y el Zoo de Fósiles. Gracias.”
Daniel Dominguez Morales
“Muchas gracias por su dedicación.”
Anónimo
Jorge Andres-Martin
Daniel Cesar Roman
“Mecenas”
José Manuel Illescas Villa
“Gracias por vuestra gran labor”
Ulrich Menzefrike
“Donación porque me gustan sus podcasts”
Francisco Ramos
Emilio Rubio Rigo
Vicente Manuel CerezaClemente
“Linfocito Tcd8”
Enrique González González
“Gracias por vuestro trabajo.”
Andreu Salva Pages
Emilio Pérez Mayuet
“Muchas gracias por vuestro trabajo”
Daniel Navarro Pons
“Por estos programas tan intersantes”
Luis Sánchez Marín
Jesús Royo Arpón
“Soy de letras, sigo reciclándome”
Fernando Alejandro Medina Vivanco
“Ayuda”
Anónimo
Fernando Vidal
José V González F
“A nombre de mi hijo León Emiliano hacemos esta pequeña aportación. Escuchar ciencia juntos nos hace muy felices. Gracias.”
Javier Galán Cantero
“Por los grandes programas, gracias”